2023年12月26日
HPV検査単独法で細胞診はどう変わるかーバイオロジーと形態から考える
さる11月5日に福岡市国際会議場で開催された第62回日本臨床細胞学会秋期大会の最後のプログラムである細胞診専門医セミナーで講演をする機会をいただきました。
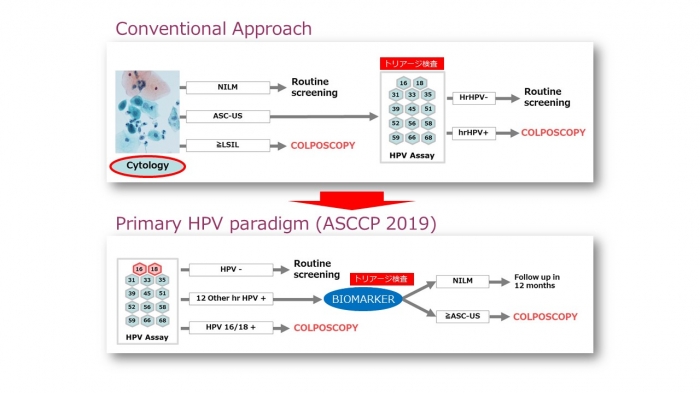
子宮頸がん検診における細胞診の位置づけが、Human papillomavirus(HPV)検査単独法の導入により変わろうとしています。その背景にはHPVの生物学的特性と扁平上皮内病変squamous intraepithelial lesion(SIL)の自然歴に関する知見の集積があることはいうまでもありません。従来のパパニコロウ Papanicolaou 分類からベセスダシステムBethesda system への移行により、細胞診の役割は形態に基づく厳密な病変推定からリスク評価へと変わりました。ベセスダシステムの本質は【感染性の異型】、すなわちコイロサイトーシスkoilocytosisという形態的バイオマーカーと【腫瘍性の異型】を認識することによる高度病変の検出です。しかし、形態認識、つまり細胞変化から HPV 感染状態にあるか否かを判定することの限界が以前から指摘されていた。その一方で、HPV の型判定 genotyping による進展リスク評価の有効性が示されたことから、近年は欧米諸国を中心に HPV 検査単独法が検診に導入されるようになりました。HPV DNA の組み込みにより E6、E7 が p53、RB 蛋白を不活化して細胞の不死化と自律的無制限の増殖を惹起し、ゲノム不安定性および変異・異常の蓄積が生じ、やがて浸潤能および転移能を獲得して扁平上皮癌に至るわけですが、これら一連のプロセスを細胞形態は必ずしも正確に反映しません。特に初期段階である LSIL/CIN1 の進展リスク評価は細胞診では困難で、偽陰性も少なくありません。こうした事実を踏まえ、最近の SGO/ASCCP のガイドラインでは、HPV 検査により 16 型、18 型が検出された場合は精査、16、18 型以外の12のハイリスク HPV が検出された場合は細胞診を実施するアルゴリズムが示されています。将来的にはp16/Ki-67 二重免疫細胞化学やより洗練されたバイオマーカーが細胞診に代わる可能性もあり、実際にそれを実証する研究の結果も示されています。しかしながら、ここで強調したいのは、細胞診および細胞診を担う細胞検査士の役割がなくなるわけではないということです。
将来的には子宮頸癌検診はバイオマーカーに基づいたアルゴリズムが主流となるでしょう。しかしながら、精度管理を含めてこれまで以上に子宮頸がん検診における細胞検査士および細胞診専門医が果たす役割は高度化していくであろう、という言葉で講演を締めくくりました。
2023年12月25日
病理医の視点から婦人腫瘍学の未来を考える-『多次元的病理学 multidimensional pathology』を見据えて
臨床医学の父と呼ばれているウイリアム・オスラー(1849-1919)の「As is pathology, so is our practice」という言葉が見事に表しているように、最適な治療は正しい病態理解、すなわち病理診断を前提とする。従って、婦人科腫瘍学は婦人科病理学とともに発展してきたといっても過言ではありません。婦人科病理学はきら星のように輝く先人たちの精緻な形態観察と洞察、治療に対する患者の反応と転帰の解析などにより形づくられ、分類体系が構築されてきました。これには病理医のみならず婦人科医の貢献が大きく、特にその黎明期においては病理学者としての資質を兼ね備えた婦人科医達が婦人科病理学の進歩の原動力となりました。
婦人科病理学は高度に臨床病理学的であり、境界悪性腫瘍やインプラント、子宮内膜増殖症に代表されるような独特の、あるいは病理総論から逸脱した概念や用語、診断基準が用いられる疾患が少なくありません。そのため、一般の病理医にとってはこの専門領域が敷居の高いものとなっている一方で、魅力ある分野ともなっています。日常の診療および医学研究において病理医と婦人科医の連携は必要不可欠で、両者の関係はゲノム医療が本格的となった今日、ますます強化されていかなければなりません。
2020年に上梓された世界保健機関(WHO)による女性生殖器腫瘍の分類第5版は、近年の研究により集積された分子遺伝学的知見と臨床病理学的知見が反映された事実上の世界標準で、日常診療および医学研究のほか、対がん戦略立案のための基礎資料である疫学データに反映されるがん登録においても不可欠で、病理医・婦人科医にとどまらず、基礎医学研究者を含む医学・医療関係者の共通言語あるいは共有財産であるといえます。従って、婦人科腫瘍の分類体系は客観的なエビデンスに基づいて構築される必要があるのと同時に、平易でユーザー・フレンドリーであることも求められます。特に病理医にとっては高い診断者間再現性が担保されることが重要で、診断基準(クライテリア)は明確である必要があります。網羅的な遺伝子発現プロファイリングはこれまで単一の組織型であると考えられていた癌腫が多彩な腫瘍群であることを明らかにし、個別化医療という観点からも腫瘍の細分化されて分類の高度化が進んでいます。既に子宮体部では類内膜癌の分子亜型がWHO分類第5版に採用され、これに基づいたリスク評価がESGOによりガイドラインとして提案されており、FIGO進行期分類にも導入されようとしています。かつてWHOによる腫瘍分類は【組織分類 histological typing】でした。しかし、今日的には、臨床病理学的特徴、画像、疫学、組織発生、分子遺伝学的背景、予後、など多くの要素によって構成される【多次元的分類 multidimensional classification】となっています。この方向性は WHO の明確な意思の現れといえますが、問題が全くないわけではありません。それは【分類】と【診断】の乖離です。
腫瘍分類の最適化あるいは再構成は患者の利益を最大化するためにも必要不可欠であることはいうまでもありませんが、病理診断を含む実地診療および医療資源とのバランスも考慮されなければなければなりません。その意味において、今まさに分類体系と診断基準のあり方が問われていると私は考えています。